Змінити пароль!
Скинути пароль!


У цьому рандомізованому дослідженні II фази вивчали безпеку введення вакцини RSVPreF3 для матерів та їх дітей, а також її імуногенні властивості. Крім того, проводили оцінку титрів антитіл до антигенів РСВ та нейтралізуючих антитіл (нАТ) у дітей, народжених імунізованими матерями.
Імунізація з введенням однієї дози експериментальної вакцини проти респіраторно-синцитіального вірусу (РСВ) (RSVPreF3) наприкінці 2-го і в 3-му триместрі вагітності добре переносилася і мала прийнятний профіль безпеки з точки зору розвитку небажаних явищ, пов'язаних з вагітністю і станом новонароджених , і навіть з погляду результатів вагітності.
У цьому рандомізованому дослідженні II фази вивчали безпеку введення вакцини RSVPreF3 для матерів та їх дітей, а також її імуногенні властивості. Крім того, проводили оцінку титрів антитіл до антигенів РСВ та нейтралізуючих антитіл (нАТ) у дітей, народжених імунізованими матерями.
Безпеку імунізації з введенням вакцини RSVPreF3 у дозі 60 або 120 мкг наприкінці 2-го та 3-го триместрів вагітності оцінювали за участю 213 здорових вагітних віком від 18 до 40 років. Обстеження матерів продовжували протягом 6 місяців після пологів, а їхніх дітей протягом перших кількох місяців життя. Імуногенність оцінювали до 43 дня після пологів у матерів і до 181 дня після народження у дітей.
Безпека імунізації з введенням вакцини RSVPreF3 була прийнятна, оскільки жодне з серйозних небажаних явищ як у вагітних, так і у дітей не було пов'язане із застосуванням вакцини, що вивчається. Основні показники, що вивчаються, були досягнуті в обох групах (введення вакцини RSVPreF3 в дозі 60 або 120 мкг).
• Через місяць після введення вакцини у матерів було виявлено підвищення титрів нАТ до антигенів підтипів РСВ-А та РСВ-В. Через 1 місяць після імунізації у матерів титри нАТ до антигену підтипу РСВ-A підвищилися у 12,7 та 14,9 раза, а до антигену підтипу РСВ-B – у 10,6 та 13,2 раза відповідно. На 43-й день після пологів титри нАТ зберігалися підвищеними у 8,9–10,0 рази порівняно зі значеннями до імунізації (див. рисунок 1).
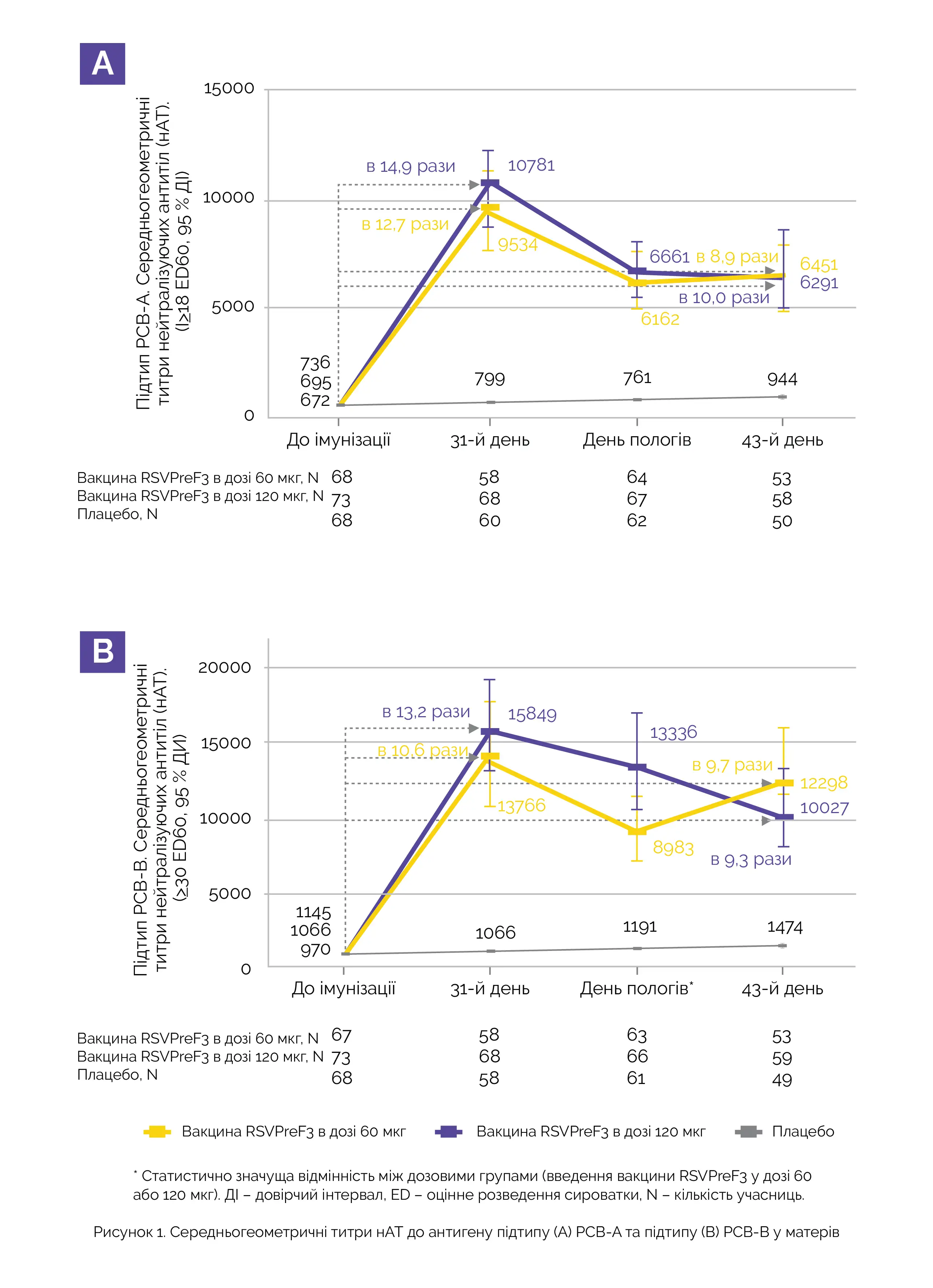
• Титри нАТ у групах, що пройшли імунізацію, були стабільно статистично значущими в порівнянні з групою плацебо.
• У групах введення вакцини RSVPreF3 у дозі 60 та 120 мкг співвідношення титрів антитіл у сироватці матері та дитини (плацентарне перенесення) при народженні склало 1,62 та 1,90 відповідно.
• Максимальний титр нАТ у дітей був присутній при народженні з поступовим зниженням протягом 181 дня.
Імунізація вагітних вакциною RSVPreF3 добре переносилася і мала прийнятний профіль безпеки. Вона забезпечувала стійку специфічну імунну відповідь проти РСВ з позитивним плацентарним переносом антитіл від імунізованих матерів їхнім дітям.
The Journal of Infectious Diseases
Safety and Immunogenicity of an Investigational Respiratory Syncytial Virus Vaccine (RSVPreF3) in Mothers and Their Infants: A Phase 2 Randomized Trial
Zourab Bebia і співавт.
Коментарі (0)